لقد وصف الطبيب السويدي أوكرمان “Okerman” المرض لأول مرة في عام 1967، ويُعد المرض واحدًا من مجموعة واسعة من اضطرابات الاختزان في الجسيمات الحالة، الناتجة عن طفرات تصيب إنزيم الألفا مانوسيداز في الجسيمات الحالة، مما يؤدي إلى نقص الإنزيم. هذا الإنزيم من الجليكوسيدات الخارجية، التي تقسم بقايا المانوز ذات روابطألفاالمتعلقة بالسكريات قليلة التعدد ذات الروابط النيتروجينية.3
الشكل 1 أ. يقسم إنزيم ألفا مانوسيداز بقايا المانوز ذو روابط الألفا المتعلقة بالسكريات قليلة التعدد ذات الروابط النيتروجينة.
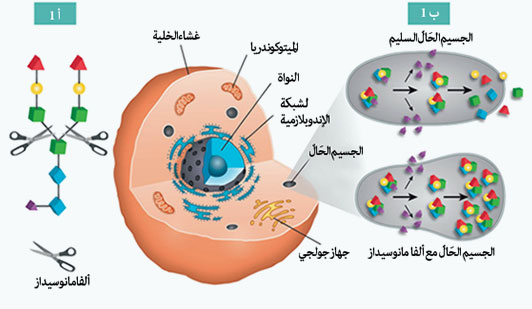
الشكل 1 ب. في الخلايا السليمة، يعمل إنزيم ألفا مانوسيداز الموجود داخل الجسيمات الحالة على التحلل التسلسلي للبروتينات السكرية المعقدة. تغادر منتجات التحليل الأصغر حجمًا الجسيم الحال. في مرض نقص ألفا مانوسيداز، يؤدي تراكم الألفا مانوسيل الغني بالسكريات قليلة التعدد ذات الروابط النيتروجينية إلى تحفل الجسيمات الحالة واضطراب وظائف الخلية الطبيعية.
ينتج مرض نقص ألفا مانوسيداز عن طفرات وراثية في جين “MAN2B1” (LAMAN) الذي يحمل شفرة إنزيم الألفا مانوسيداز الموجود في الجسيمات الحالة4A. يُعد مرض نقص ألفا مانوسيداز من الأمراض ذات الوراثة الجسدية المتنحية. يتكون جين “MAN2B1” من 24 إكسون ويحمل شفرة 1011 حمض أميني متعدد البيتيد الذي يتم تعديله بعد مرحلة الترجمة في الشبكة الإندوبلازمية5A. أثناء نضج جين “MAN2B1” وانتقاله الداخلي إلى الجسيمات الحالة، يتحلل بروتينيًا إلى ثلاثة أشكال رئيسية من متعددات البيتيدات تحمل اسم “abc” و”d” و”e” بحجم 70 و42 و15 كيلو دالتون، على التوالي6. بشكل أكثر تحديدًا ، ينتج عن معالجة الوحدة الفرعية ذات حجم 70 كيلو دالتون إلى خمسة من متعددات البيتيد المختلفة بشكل إجمالي. يظهر أعلى مستوى لجين “MAN2B1” في الرئة والكلى والبنكرياس وخلايا الدم البيضاء في الدم المحيطي7A. في الجهاز العصبي المركزي، يظهر أعلى مستوى له في الجسم الثفني والحبل الشوكي، بينما يُلاحظ وجود مستويات أقل في الأجزاء الأكبر، التي تشمل المخيخ والقشرة المخية والفص الجبهي والفص الصدغي. على الرغم من ذلك، من غير الواضح في الوقت الحالي أهمية هذه الاختلافات (إن وُجدت)7A.
تتسبب الطفرات الموجودة في جين “MAN2B1” إلى تعطيل نشاط إنزيم الألفا مانوسيداز داخل الجسيمات الحالة8A. بناءً على طفرة جين “MAN2B1” المتسببة في الأمر، تم الكشف عن بروتينات “MAN2B1” الطافرة في المقصورات تحت الخلوية مثل الشبكة الإندوبلازمية أو الجسيمات الحالة9A. على سبيل المثال، يُمكن أن يُطوى البروتين بصورة غير سليمة ويُحتجز في الشبكة الإندوبلازمية، أو يُمكن أن يُطوى بصورة سليمة وينتقل إلى الجسيمات الحالة في صورة غير نشطة10A. لقد تم حتى الآن تحديد 155 نوعًا مختلفًا لدى 191 مريض وقد تم وصفهم بصورة جزئية على المستوى البيوكيميائي11A.
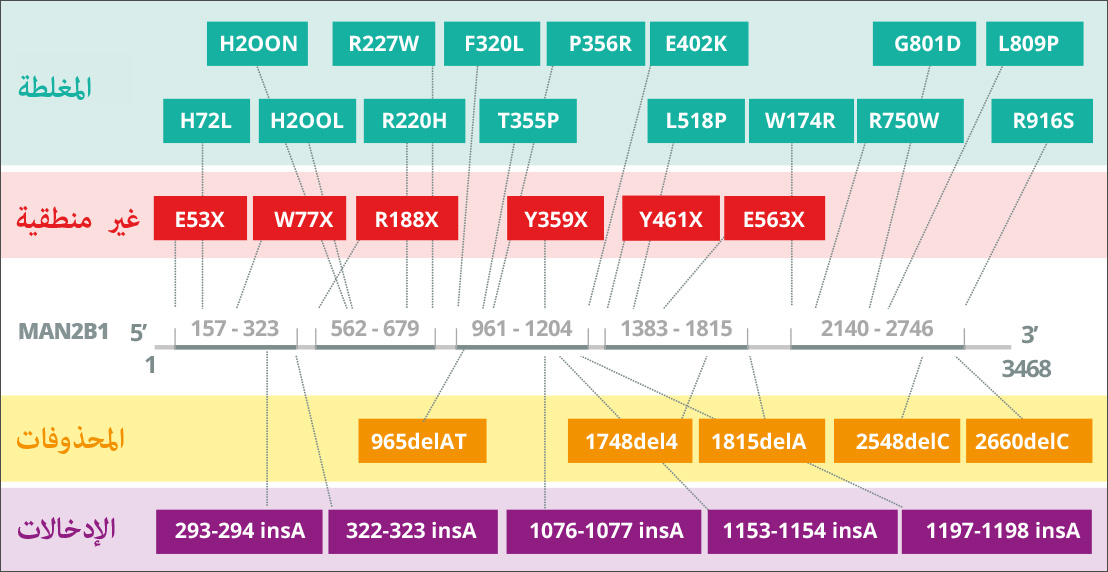
إذا كان إنزيم ألفا مانوسيداز ضعيفًا، سوف يحدث إنخفاض في تحليل البروتينات السكرية وتراكم تدريجي للسكريات قليلة التعدد الغنية بالمانوز في كافة الأنسجة، مما سوف يؤدي إلى ضعف عمل الخلايا والاستماتة “الموت المبرمج للخلية.13 يُورث مرض نقص ألفا مانوسيداز بطريقة جسدية متنحية، نتيجة لطفرات في الجين “MAN2B1″، الموجود على الكروموسوم 19. يرتفع معدل التقلب المظهري، حتى بين الأشقاء الذين تتطابق أنماطهم الجينية14. بالإضافة إلى العوامل الوراثية، قد تؤثر العوامل البيئية على المرض. على سبيل المثال، قد يؤدي التعرض لمسببات الأمراض إلى تكرار العدوى وتفاقم أعراض المرض.15
– إن الغرض من المعلومات الواردة على الموقع الإلكتروني هو توفير المعرفة بالموضوعات الصحية المتعلقة بمرض نقص ألفا مانوسيداز فحسب. لا ينبغي استخدام هذه المعلومات بدلًا من استشارة طبيبك العام أو أي متخصص أخر في الرعاية الصحية. إذا كانت تساورك الشكوك، يُرجى الاتصال بطبيبك للحصول على النصيحة. تم إنتاج هذا الموقع بواسطة شركة كييزي فامارتشوتشي “CHIESI Farmaceutici “ لقد تم تطوير هذا الموقع الإلكتروني طبقًا للمعايير الصناعية والقانونية لتوفير المعلومات المتعلقة بالموضوعات الصحية لمرض نقص ألفا مانوسيداز لخبراء الرعاية الصحية وعموم الناس. تبذل شركة كييزي فامارتشوتشي “CHIESI Farmaceutici” ما بوسعها من جهود معقولة من أجل تضمين معلومات دقيقة وحديثة. ومع ذلك، إن المعلومات الواردة في هذا الموقع الإلكتروني ليست شاملة.